Este é o nono estudo de vacina contra Covid-19 autorizado pela Anvisa para o Brasil.
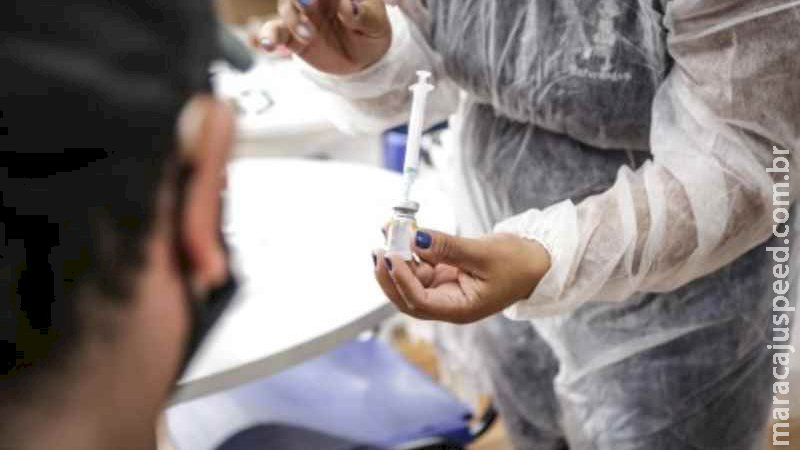
A Anvisa aprovou, nesta terça-feira (6/7), uma nova pesquisa clínica de vacina contra Covid-19, que deverá ser testada no país, desenvolvida pela Sanofi Pasteur. Os testes vão ser feitos em 150 voluntários com 18 anos ou mais de Mato Grosso do Sul, da Bahia, Minas Gerais e Rio de Janeiro.
Segundo divulgou a agência, a vacina candidata usa uma tecnologia de RNAm (RNA mensageiro) encapsulado dentro de uma nanoarticulação lipídica (LNP) que protege o RNAm da degradação. A vacina é a MRT1500 RNAm (ácido ribonucleico mensageiro)
O estudo clínico será de fase 1/2 e tem como objetivo testar três diferentes dosagens da vacina para definir a dose ideal antes de prosseguir para um estudo de fase III.
O estudo prevê a aplicação de duas doses, com 21 dias de intervalo, e será conduzido nos estados citados. O início dos testes depende apenas da apresentação dos resultados dos estudos de estabilidade da vacina, que definem o prazo de validade do produto.
No mundo o ensaio de fase 1/2 está deve acontecer também nos EUA, Honduras e Austrália. A candidata à vacina com o diluente será fabricada pelas empresas Translate Bio sediada nos Estados Unidos, a empresa Evonik Canada Inc. (Evonik Vancouver Laboratories), situada no Canadá, e a empresa Sanofi Pasteur, sediada na França e nos Estados Unidos.
Este é o nono estudo de vacina contra Covid-19 autorizado pela Anvisa para o Brasil. As outras pesquisas já autorizadas são da Pfizer, Astrazeneca, Coronavac, Janssen, Clover, Medicago, Janssen e Covaxin.






Olá, deixe seu comentário!Logar-se!